Иммунотерапия при опухолях мозга у детей и взрослых

Бывают случаи, когда при опухоли мозга стандартные протоколы лечения не работают или состояние пациента не позволяет их продолжать, например из-за стадии болезни или побочных эффектов. Поэтому специалисты разрабатывают и применяют новые методы борьбы с болезнью. Один из них — иммунотерапия.
В этой статье мы расскажем о принципе работы иммунотерапии, ее основных видах и показаниях к назначению. А еще о том, как проходит лечение, и о возможных побочных эффектах.
Что такое иммунотерапия и в чем сложности ее применения при опухолях мозга

Иммунотерапия — это метод лечения, при котором организм использует свою собственную защиту, стимулирует или подавляет иммунную систему, помогая ей находить и уничтожать мутировавшие клетки.
Несмотря на то, что иммунотерапия — перспективный метод лечения онкозаболеваний, который активно развивается, его применение при опухолях мозга сталкивается с рядом сложностей:
- Мозг — «иммунопривилегированный» орган. У него есть естественные защитные механизмы — «охранники», например клетки микроглии (один из видов иммунных клеток центральной нервной системы), которые регулируют воспалительные процессы и следят, чтобы иммунные клетки не вели себя слишком активно. Это хорошо для обычной жизни, но когда в мозге появляется опухоль, эти «охранники» мешают иммунотерапии, поскольку подавляют работу тех самых клеток, которые должны бороться с новообразованием.
- Гематоэнцефалический барьер (ГЭБ). Это сложный фильтр внутри сосудов головного мозга. Его образуют стенки капилляров вместе с особыми клетками — перицитами и астроцитами, — которые плотно прилегают к тканям. Барьер тянется вдоль всего лабиринта сосудов и строго отбирает вещества, которые могут попасть из крови в мозг. ГЭБ способен мешать иммунотерапевтическим препаратам достигать опухоли в нужном объеме.
- Сходство опухолевых клеток со здоровыми. Опухолевые клетки часто маскируются под обычные, что затрудняет их распознавание иммунной системой. Кроме того, опухоли могут вырабатывать сигналы, которые подавляют иммунный ответ или обманывают его, что напрямую снижает эффективность иммунотерапии. Лекарства, которые должны помочь иммунитету бороться с опухолью, либо не видят ее, либо опухоль активно подавляет их действие.
Несмотря на эти сложности, ученые активно работают над усовершенствованием иммунотерапии и поэтому этот метод лечения показывает хорошие результаты у части пациентов. Сегодня исследуются сочетания разных видов иммунотерапии и новые методы доставки лекарств.
Виды иммунотерапии, которые применяются при опухолях мозга
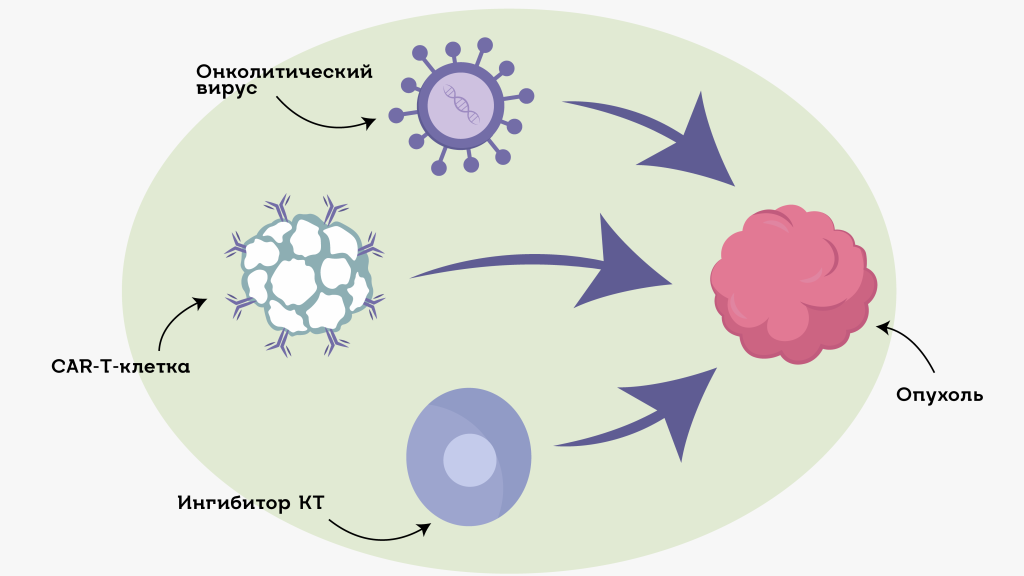
Чтобы активировать иммунитет для борьбы с опухолью, врачи используют разные подходы: от «умных» лекарств до генетически измененных вирусов. Среди основных:
Моноклональные антитела
Это прицельная терапия, которая находит слабые места в опухолевых клетках и прерывает сигналы, которые помогают им расти. У этого метода есть несколько видов терапии:
- Ингибиторы контрольных точек. Вид моноклональных антител, которые мешают опухоли «прятаться». В норме белки вроде PD-1 или CTLA-4 сообщают иммунитету, что клетку трогать не нужно. Опухоль использует эти белки, чтобы обмануть защиту организма. Ингибиторы блокируют этот механизм, «снимают маскировку» с новообразования и позволяют Т-клеткам начать атаку.
- Конъюгаты. Антитела, которые работают как курьеры. Они доставляют прямо к опухоли токсин или радиоактивный элемент, который уничтожает ее клетки, минимально задевая здоровые.
Онколитические вирусы
Онколитические вирусы — это, как правило, генетически измененные вирусы, которые атакуют клетки новообразований и не трогают здоровые. Вирус проникает в опухолевую клетку и разрушает ее. Этот процесс провоцирует воспаление, которое нарушает микроокружение опухоли и лишает ее возможности маскироваться под нормальную ткань. Сочетание воспаления и высвобожденных опухолевых антигенов после разрушения клеток помогает иммунной системе увидеть врага и начать атаку. Также вирус запускает апоптоз — процесс самоуничтожения мутировавших клеток.
Клеточная иммунотерапия
В этом случае врачи используют собственные клетки пациента, чтобы усилить защитный ответ.
- CAR-T-клетки. Т-клетки пациента перепрограммируют в лаборатории, чтобы они лучше находили специфические метки на опухоли. Метод пока проходит клинические испытания для лечения опухолей мозга (например, диффузных срединных глиом).
- Дендритноклеточные вакцины. Клетки пациента «обучают» в лаборатории распознавать компоненты опухоли и возвращают обратно, чтобы они запустили мощную иммунную реакцию.
Комбинированная терапия
При выборе такой тактики лечения используется несколько иммунотерапевтических подходов одновременно. Например, сочетают ингибиторы контрольных точек с онколитическими вирусами или CAR-T-клеточной терапией. Такой многосторонний подход помогает преодолеть сложности, связанные с иммуноподавляющей средой вокруг опухоли мозга, и повысить эффективность лечения.
Когда назначают иммунотерапию

В случае, если стандартные методы лечения опухоли мозга — операция, лучевая или химиотерапия — оказались неэффективными или прогноз с использованием стандартных методов лечения неблагоприятный, могут назначить иммунотерапию. Такая терапия считается особенно актуальной для агрессивных образований вроде глиобластомы, которая быстро растет и плохо поддается стандартному лечению.
На выбор в пользу назначения иммунотерапии при опухоли мозга влияет несколько моментов:
- Вид опухоли: иммунотерапию рассматривают при некоторых видах опухоли, обладающих особенностями, на которые может воздействовать иммунная система. Часто это происходит в рамках клинических исследований, особенно при рецидиве.
- Молекулярные особенности опухоли: наличие на поверхности опухоли определенных белков или генетические изменения, которые способны сделать ее уязвимой для иммунотерапии.
- Общее состояние здоровья пациента: необходимо убедиться, что организм пациента сможет перенести такое лечение, потому что иммунотерапия может вызывать побочные эффекты и перегрузить ослабленный организм.
В лечении детей иммунотерапия считается менее изученным методом, чем для взрослых, и чаще всего его применяют в рамках строго контролируемых клинических испытаний. Это связано с несколькими причинами:
- Различия опухолей: у детей нередко встречаются другие виды опухолей мозга, которые могут иметь иное молекулярное строение по сравнению с теми, что развиваются у взрослых.
- Развитие иммунитета: детская иммунная система еще находится в процессе формирования. Это может влиять на то, как организм ребенка отреагирует на иммунотерапию и как он переносит препараты.
- Забота о будущем: врачи уделяют особое внимание тому, как лечение может повлиять на растущий организм и развивающийся мозг ребенка в долгосрочной перспективе, стремясь снизить любые потенциальные риски.
Денис Корнеев, детский онколог:
— В педиатрии иммунотерапию используют редко. К ней обращаются в исключительных случаях, когда возможности стандартных протоколов лечения исчерпаны, либо если диагностика подтверждает специфические маркеры. Например, высокую микросателлитную нестабильность и наличие большого количества белка PD-L1. Они говорят о том, что иммунотерапия в случае пациента будет эффективна.
Как проходит иммунотерапия при опухоли мозга
Иммунотерапия проводится только в клинике. Домашнее лечение исключено из-за риска острых реакций, которые требуют немедленной помощи. В редких случаях встречаются быстро развивающиеся аллергические реакции (отек Квинке, бронхоспазм, анафилактический шок), которые требуют срочного введения препаратов и поддержания дыхания.
Лекарства иммунотерапии, как правило, вводятся внутривенно. Процедура может занимать время, потому что некоторые препараты нужно вводить медленнее, чем другие. Также чем больше его объем, тем дольше может длиться вливание. В некоторых случаях врач может корректировать скорость введения, если у пациента возникают нежелательные реакции.
При применении онколитических вирусов и дендритноклеточных вакцин возможно введение непосредственно в спинномозговую жидкость: инъекция в спинной мозг или через специальное устройство (резервуар Оммайя) в желудочки головного мозга. В таких случаях процедура проходит быстро.
Денис Корнеев:
— Режим проведения иммунотерапии регламентирован инструкциями к конкретным препаратам. Длительность курса не ограничена фиксированным количеством сеансов — лечение продолжается до тех пор, пока сохраняется положительная динамика в лечении и отсутствуют непереносимые побочные эффекты.
Побочные эффекты иммунотерапии

Среди частых побочных эффектов могут быть:
- сильная усталость, которая не проходит после отдыха;
- повышенная температура;
- мышечные или суставные боли, как при простуде;
- кожные реакции: зуд, покраснения или высыпания;
- тошнота или потеря аппетита.
Однако реже могут возникать более серьезные побочные эффекты, когда иммунная система чрезмерно реагирует и вызывает воспаление в различных органах. К ним относятся:
- воспаление в кишечнике (колит), который проявляется сильной диареей;
- неинфекционное воспаление легких (пневмонит), что вызывает одышку и кашель;
- нарушение работы щитовидной железы (тиреоидит), которое влияет на гормональный фон;
- аллергические реакции, в том числе отек Квинке (ангионевротический отек).
Также существует небольшая вероятность воспаления самого головного мозга (энцефалита) или его оболочек (менингита). Это может проявиться в виде сильных головных болей, изменений в поведении, спутанности сознания или судорог.
Именно поэтому пациенты, которые проходят иммунотерапию при опухолях мозга, находятся под тщательным наблюдением. Кроме того, крайне важно незамедлительно сообщать лечащему врачу о любых новых симптомах или изменениях в самочувствии.
Источники:
- Immunotherapy https://braintumourresearch.org/blogs/types-of-brain-tumour/immunotherapy-for-brain-tumours?srsltid=AfmBOorCcYtdMtdrO3GSvwhvxbY8bMlRk78j0mHazFrMyFaW69AQSw-j
- Immunotherapy side effects https://www.facingourrisk.org/info/risk-management-and-treatment/cancer-treatment/by-treatment-type/immunotherapy/side-effects?campaign=698450
- Иммунотерапия в детской онкологии https://wiki.nenaprasno.ru/a/immunoterapiia-v-detskoi-onkologii