
Злокачественная опухоль возникает из-за мутаций в ДНК клеток, заставляющих их бесконтрольно расти, делиться и при этом скрываться от иммунной системы. Многолетние исследования показали, что этому способствуют определенные молекулярные особенности опухолевых клеток. Таргетная терапия основывается на прицельном воздействии на эти механизмы.
Как именно работает таргетная терапия? В каких случаях ее применяют и какие препараты назначают взрослым и детям с опухолями мозга? На эти и другие вопросы подробнее отвечаем в статье.
Что такое таргетная терапия
Таргетная терапия (от англ. target — «цель», «мишень») — это лекарственный метод лечения онкологических заболеваний, в том числе опухолей мозга. В отличие от химиотерапии, таргетные препараты воздействуют не на все быстро делящиеся клетки в организме, а на конкретные молекулы-мишени (например, белки или мутировавшие гены) внутри опухоли или на ее поверхности.
Блокируя механизмы действия этих молекул, таргетная терапия замедляет рост и распространение злокачественных клеток, минимизируя повреждение здоровых. Благодаря такой избирательности ее также называют молекулярно-таргетной терапией.
Мишенью для таргетных препаратов могут стать: избыточное количество определенного белка (по сравнению с нормой), мутантный белок или ген, белок в опухолевой клетке, которого нет в нормальных клетках, или специфические изменения в ДНК опухолевой клетки.
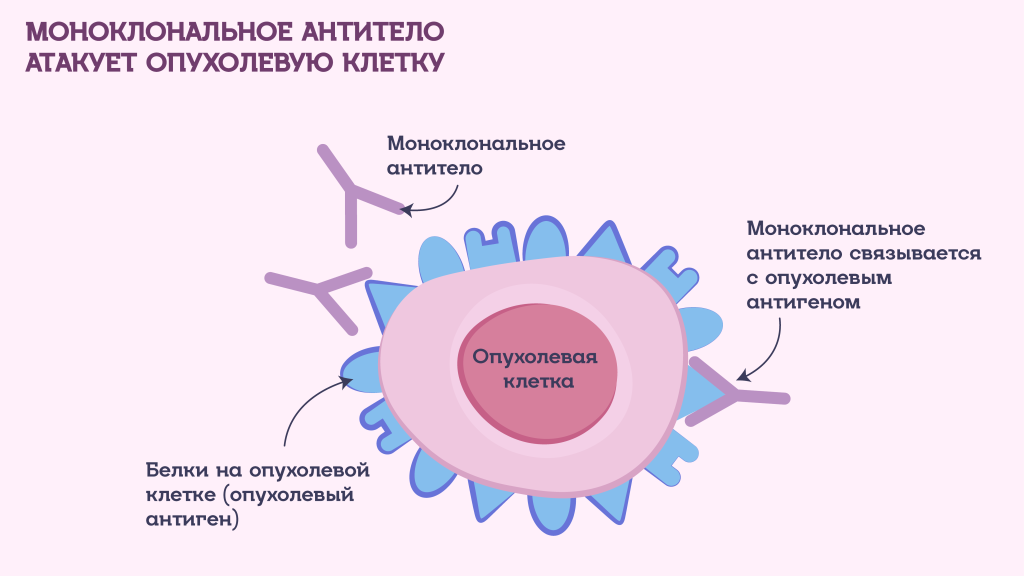
Механизмы действия таргетной терапии: блокировка сигналов роста и деления опухолевых клеток, изменение белков внутри опухоли для ее гибели, подавление образования новых кровеносных сосудов, питающих опухоль, а также активация собственной иммунной системы (принцип работы иммунотерапии).
Когда назначают таргетную терапию
На решение о назначении таргетной терапии влияют следующие факторы:
- Наличие молекулярных мишеней. Специфические мутации или белки в опухолевых клетках — обязательное условие для применения большинства таргетных препаратов. Для их выявления предварительно проводятся молекулярно-генетические исследования. Например, флуоресцентная гибридизация in situ (FISH) или комплексное геномное профилирование на основе секвенирования нового поколения (NGS).
- Тип опухоли и степень ее распространения.
- Предшествующее лечение. Как правило, врачи рассматривают вариант применения таргетной терапии, когда стандартные методы противоопухолевого лечения (операция, лучевая и химиотерапия) исчерпали себя или их применение невозможно в случае пациента.
- Общее состояние пациента. Возраст, наличие осложнений из-за опухоли и ее предшествующего лечения. Например, возможность применять препараты перорально.
- Побочные эффекты. Несмотря на меньшую токсичность в сравнении с химиотерапией, таргетная терапия также сопряжена с риском различных осложнений: например, кровотечения, образования тромбов, печеночной, кардиоваскулярной токсичности, а также угнетением костного мозга.
Побочные эффекты
Таргетная терапия теоретически не оказывает выраженного негативного влияния на здоровые клетки. Однако, воздействуя на общие со здоровыми клетками гены и белки опухоли, она не лишена побочных эффектов. При этом часто они имеют другой спектр, нежели на фоне химиотерапии или лучевой терапии.
Если же осложнения на фоне таргетной терапии возникнут, то это может случиться в любое время — в процессе лечения, сразу после него либо через несколько дней или недель. Иногда развиваются поздние побочные реакции, которые проявляются через месяцы или годы после терапии. Большинство побочных эффектов проходят сами после отмены таргетной терапии или снижения дозы препарата, а также поддаются лечению. В редких случаях они могут длиться долго или стать постоянными.
Реакции будут зависеть в основном от типа или комбинации препаратов, дозы, способа применения и общего состояния здоровья пациента. Можно выделить несколько распространенных побочных эффектов при таргетной терапии опухолей головного и спинного мозга:
- усталость;
- головная боль;
- воспаления и язвы во рту;
- потеря аппетита;
- тошнота;
- диарея;
- низкий уровень лейкоцитов (увеличивает риск инфекции);
- повышенное артериальное давление;
- кожные проблемы, такие как сыпь;
- скопление жидкости, отеки (чаще всего в ногах);
- боль в мыщцах, суставах и костях.
Какие таргетные препараты широко используют для лечения пациентов с опухолью мозга
Бевацизумаб
Бевацизумаб — это искусственная версия белка иммунной системы, который относится к классу моноклональных антител. Эти антитела воздействуют на фактор роста эндотелия сосудов — белок, который помогает опухолям формировать новые кровеносные сосуды, необходимые им для роста.
В основном препарат используют для борьбы с некоторыми типами глиом (особенно для быстрорастущих глиобластом), которые рецидивируют после стандартного противоопухолевого лечения. Также его применяют для борьбы с менингиомами.
У бевацизумаба есть возрастное ограничение: согласно инструкции его применение не рекомендовано пациентам до 18 лет, однако врачи могут назначить его и детям по строгим жизненным показаниям (офф-лейбл, англ. off-label, от off — за пределами, label — этикетка, инструкция).
Эверолимус
Эверолимус блокирует клеточный белок, который обычно помогает клеткам расти и делиться. Его используют для лечения субэпендимальных гигантоклеточных астроцитом, которые невозможно полностью удалить хирургическим путем.
У эверолимуса также есть возрастное ограничение применения до 18 лет, и врачи могут его назначить детям по строгим жизненным показаниям.
Ларотректиниб, энтректиниб и репотректиниб
Эти препараты нацелены на определенное генетическое изменение, которое называют слиянием генов NTRK. Оно встречается в нескольких типах опухолей, включая некоторые виды опухолей мозга.
Ларотректиниб, энтректиниб и репотректиниб также могут применяться для лечения детей старше 12 лет.
Дабрафениб и траметиниб
Препараты, которые воздействуют на белки BRAF и MEK. Они также могут быть назначены несовершеннолетним пациентам при наличие медицинских показаний. Например, сочетание этих препаратов используют для лечения детей старше одного года с любым типом глиомы низкой степени злокачественности с мутацией, если опухоль требует лечения, отличного от хирургического вмешательства или лучевой терапии.
Товорафениб
Помимо взрослых пациентов, товорафениб может быть назначен и детям, начиная с 6 месяцев. Например, для лечения рецидивирующей или рефрактерной глиомы низкой степени злокачественности с мутацией гена BRAF.
Источники:
- Таргетная терапия https://nenaprasno.ru/wiki/a/targetnaia-terapiia
- Targeted drug therapy for adult brain and spinal cord tumors https://www.cancer.org/cancer/types/brain-spinal-cord-tumors-adults/treating/targeted-therapy.html
- Brain tumors: targeted therapy https://www.urmc.rochester.edu/encyclopedia/content?contenttypeid=34&contentid=17822-1
- Targeted therapy drugs for brain and spinal cord tumors in children https://www.cancer.org/cancer/types/brain-spinal-cord-tumors-children/treating/targeted-therapy.html
- FDA grants accelerated approval to tovorafenib for patients with relapsed or refractory BRAF-altered pediatric low-grade glioma https://www.google.com/url?q=https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-repotrectinib-adult-and-pediatric-patients-ntrk-gene-fusion-positive&sa=D&source=docs&ust=1773670846535032&usg=AOvVaw1MvIC7wU98PU79jhmuuiAB